Wednesday, 12:07 06/10/2021
|
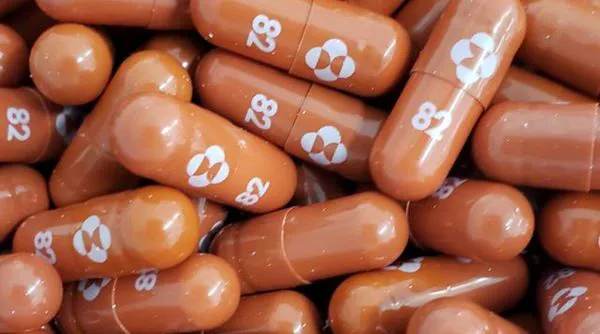
| Thuốc viên Molnupiravir thử nghiệm điều trị Covid-19. Ảnh: Reuters |
Reuters ngày 5/10 dẫn lời quan chức của Cơ quan Dược phẩm Châu Âu (EMA) cho biết, EMA đang xem xét thực hiện một đợt đánh giá tổng hợp đối với Molnupiravir - thuốc viên điều trị Covid-19 đang trong quá trình thử nghiệm của hãng dược phẩm Merck (Mỹ), kết hợp với công ty Ridgeback Biotherapeutics (Đức) điều chế.
Trước đó, Merck đã công bố kế hoạch xin cấp phép sử dụng khẩn cấp (EUA) từ Cơ quan Quản lý Dược phẩm Mỹ để sử dụng Molnupiravir làm thuốc kháng virus SARS-CoV-2. Công ty cũng có kế hoạch nộp đơn đăng ký tiếp thị cho các cơ quan quản lý trên toàn thế giới.
Nếu thành công, Molnupiravir có thể trở thành thuốc điều trị Covid-19 đường uống đầu tiên được cấp phép. Hiện, Molnupiravir đang được thử nghiệm trong phác đồ điều trị của nhiều quốc gia, bao gồm Việt Nam.
Tại Ấn độ, Merck đã sớm liên kết với 8 công ty quốc nội để sản xuất Molnupiravir ở nước này. Theo Tiến sĩ Shekhar Mande, Chủ tịch Hội đồng Nghiên cứu Khoa học và Công nghiệp Ấn Độ (CSIR), khi hướng tới việc "sống chung với Covid-19", thuốc kháng virus dạng uống sẽ đóng một vai trò quan trọng trong việc hỗ trợ điều trị các ca bệnh.
"Trong khi chờ đợi các đánh giá chuyên ngành, dựa trên các báo cáo, Molnupiravir có vẻ đầy hứa hẹn và sẽ cung cấp một lựa chọn tốt", ông Mande nói với The Indian Express.
Theo phân tích tạm thời được công bố hồi tuần trước, Molnupiravir được thông báo có khả năng làm giảm khoảng 50% nguy cơ nhập viện và tử vong vì Covid-19. Khoảng 7,3% bệnh nhân dùng Molnupiravir phải nhập viện hoặc tử vong cho đến ngày 29 sau khi phân tích ngẫu nhiên, so với mức 14,1% bệnh nhân được điều trị bằng giả dược. Qua ngày 29 sử dụng thuốc, không có trường hợp tử vong nào được báo cáo ở những bệnh nhân dùng molnupiravir, so với 8 trường hợp tử vong ở những bệnh nhân dùng giả dược.