Giảm thủ tục cấp phép khẩn cấp cho vaccine Nanocovax: Vaccine phòng Covid-19 Nanocovax được Công ty CP Công nghệ sinh học dược Nanogen phát triển từ tháng 5/2020, dựa trên công nghệ protein tái tổ hợp. Trước khi thử nghiệm giai đoạn 3, vaccine này đã trải qua 2 giai đoạn thử nghiệm lâm sàng: Giai đoạn 1 bắt đầu từ ngày 18/12/2020, giai đoạn 2 từ ngày 26/2/2021 và giai đoạn 3 chính thức từ ngày 11/6/2021.
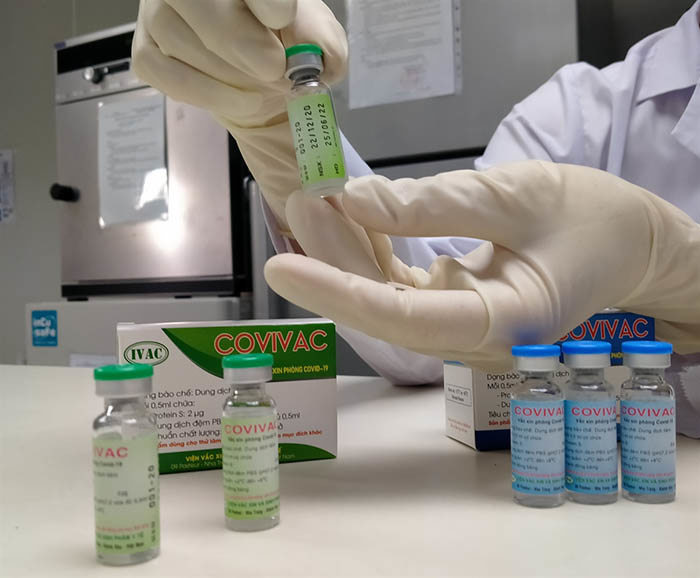
Theo đề cương đã được phê duyệt, giai đoạn 3 tiêm thử nghiệm vaccine Nanocovax nhằm đánh giá yếu tố hiệu lực bảo vệ của vaccine đối với cộng đồng và được thực hiện tại nhiều trung tâm trong nước với 13.000 người; chỉ thực hiện tiêm nhóm liều duy nhất 25mcg và nhóm tiêm giả dược đối chứng. Qua 2 giai đoạn đầu, kết quả thử nghiệm cho thấy, 100% tình nguyện viên đều sinh miễn dịch tốt. Tỷ lệ chuyển đổi huyết thanh đạt trên 99%. Trước những nghiên cứu khả quan của Nanocovax, Thủ tướng giao Bộ Y tế nghiên cứu, đề xuất theo thẩm quyền, bảo đảm quy trình chặt chẽ, an toàn, hiệu quả và rút gọn thủ tục hành chính về cấp phép khẩn cấp cho vaccine Nanocovax.Liên quan đến vaccine này, cuối tuần qua, Giám đốc điều hành Công ty Vekaria Healthcare LLP của Ấn Độ, cùng với ông Hồ Nhân - Tổng Giám đốc Công ty Nanogen của Việt Nam, đã ký Bản Thỏa thuận giữ Bí mật (Non-Disclosure Agreement, NDA) nhằm phục vụ chuyển giao công nghệ, sản xuất và phân phối vaccine Nanocovax. Việc ký thỏa thuận NDA sẽ là cơ sở để hai bên tiến tới thảo luận sâu hơn về các nội dung hợp tác cụ thể liên quan đến sản xuất, phân phối vaccine Nanocovax quy mô lớn khi các cơ quan chức năng cấp phép sử dụng khẩn cấp. Theo đánh giá của đại diện công ty Vekaria Healthcare, vaccine Nanocovax được nghiên cứu, phát triển trên nền tảng công nghệ protein tái tổ hợp, các báo cáo nghiên cứu ban đầu cho thấy, vaccine này có nhiều triển vọng.Covivac bắt đầu thử nghiệm giai đoạn 2: Vaccine Covid-19 Covivac đã bắt đầu thử nghiệm lâm sàng giai đoạn 2 trên 375 tình nguyện viên ở Thái Bình với nhóm liều 3mcg và 6mcg và một nhóm tiêm giả dược. Trước đó, Hội đồng đạo đức, Bộ Y tế đã họp đánh giá giai đoạn 1 vaccine Covivac, kết luận vaccine an toàn, dung nạp tốt, có tính sinh miễn dịch, đủ điều kiện chuyển sang giai đoạn 2.PGS.TS Vũ Đình Thiểm - Giám đốc Trung tâm Thử nghiệm lâm sàng, Viện Vệ sinh Dịch tễ Trung ương cho biết, các tình nguyện viên phải đảm bảo từ trên 18 tuổi, có thể lên tới 70 - 80 tuổi, bao gồm cả những người mắc bệnh mạn tính như tiểu đường, tăng huyết áp nhưng đang được điều trị ổn định. Nếu giai đoạn 2 diễn ra thuận lợi, đến cuối tháng 9, nhóm nghiên cứu sẽ thu được mẫu máu của các tình nguyện viên ở thời điểm ngày thứ 42 sau mũi đầu tiên để đánh giá tính sinh miễn dịch và hiệu giá kháng thể trung hòa của vaccine. Đến ngày thứ 57, các tình nguyện viên sẽ tiếp tục được khám sức khỏe, lấy mẫu máu để đánh giá, phân tích trước khi nhóm nghiên cứu đề xuất thử nghiệm giai đoạn 3a trên 1.000 tình nguyện viên.Covivac hiện là vaccine ngừa Covid-19 thứ hai của Việt Nam đang thử nghiệm lâm sàng. Vaccine sử dụng công nghệ vector virus, tương tự như vaccine AstraZeneca nhưng sử dụng giá thể khác nhau. Trong đó Covivac sử dụng vector NewCastle trên phôi trứng gà theo dây chuyền sản xuất vaccine cúm mùa, còn AstraZeneca sử dụng vector adenovirus tinh tái tổ hợp.Thử nghiệm lâm sàng vaccine VBC-COV19-154: Bộ Y tế vừa phê duyệt chương trình thử nghiệm lâm sàng vaccine VBC-COV19-154 bắt đầu tiến hành tại trường Đại học Y Hà Nội. Theo đó, VBC-COV19-154 do Công ty VinBioCare (thành viên thuộc Tập đoàn Vingroup) triển khai chuyển giao công nghệ sản xuất từ vaccine ARCT-154 của Arcturus (Mỹ). Bà Lê Ngọc Chi - Tổng Giám đốc VinBioCare cho biết, cùng với nhiều giải pháp khác và sự vào cuộc phối hợp của các bộ ngành, dự kiến, lô vaccine thương mại đầu tiên có thể ra đời vào tháng 3/2022, sớm hơn 18 tháng so với kế hoạch ban đầu nhưng vẫn bảo đảm tuân thủ chất lượng theo đúng các tiêu chuẩn quốc tế cao nhất và đúng các quy định của Bộ Y tế Việt Nam.Hiện nay, VinBiocare đã ký kết xong các hợp đồng mua sắm máy móc thiết bị. Công tác xây dựng nhà xưởng cũng đã cơ bản hoàn thành, việc lắp đặt thiết bị dự kiến sẽ kết thúc trong tháng 11/2021. Nhà máy sản xuất vaccine của VinBioCare sẽ đặt tại Tổ hợp Nhà máy sản xuất thiết bị điện tử VinSmart tại Khu công nghiệp Hòa Lạc (Thạch Thất, Hà Nội) với tổng vốn đầu tư hơn 200 triệu USD; công suất 200 triệu liều mỗi năm. Đây là một trong 5 công trình trọng điểm cấp bách được phép hoạt động trong thời gian Hà Nội thực hiện giãn cách.Với việc chuyển giao công nghệ, chủ động tự chủ được sản xuất trong nước, giá vaccine do VinBioCare dự kiến rẻ hơn so với sản phẩm cùng phân khúc đang được chào bán trên thị trường. Theo Chủ tịch Tập đoàn Vingroup Phạm Nhật Vượng, VinBioCare sẽ cung cấp vaccine phòng Covid-19 cho Việt Nam với giá chỉ có chi phí, không tính lợi nhuận trong suốt thời gian chống dịch.